Lungenfibrose (IPF): Behandlung und Therapiemethoden in der Pflege
Die Lungenfibrose ist eine schwere und unheilbare Lungenerkrankung. Basierend auf Studien rechnen Experten des European IPF Network die Zahl der Betroffenen bezüglich interstitielle Lungenerkrankungen in Europa auf ungefähr 750.000. Dieser Artikel dient als Übersicht zur Pathophysiologie, Diagnostik und den grundsätzlichen Ansätzen zur Therapie sowie der begleitenden Pflege bei Lungenfibrose.
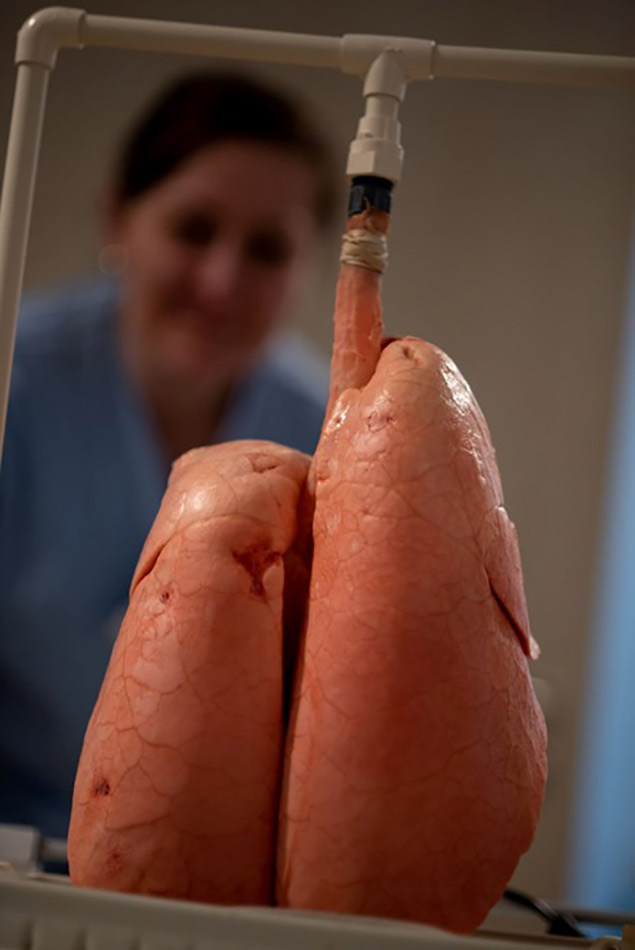
Bei der Lungenfibrose bildet sich Narbengewebe im Inneren der Lunge | © ZBI Gruppe
Was ist eine Lungenfibrose?
Die Lungenfibrose ist eine chronische Erkrankung der Lunge, insbesondere des Lungenbindegewebes. Manchmal wird auch der Begriff “Narbenlunge” benutzt. Die Bezeichnung Lungenfibrose wird von dem lateinischen Wort: “fibra”, welches für Faser steht, abgeleitet. Hinter dem Begriff Lungenfibrose stehen mehrere verschiedene Lungenerkrankungen, deren Gemeinsamkeit der Umbau von Lungengewebe ist. Durch eine vermehrte Bildung von Bindegewebsfasern vernarbt und verhärtet die Lunge buchstäblich. Dieser Vorgang wird mit dem Begriff Fibrosierung beschrieben. So wird das Interstitium, wie Lungenbindegewebe und -stützgewebe um die Lungenbläschen und die kleinen Bronchien genannt werden, dauerhaft und zum Nachteil der Lungenfunktion verändert. Ebenfalls sind die Lungenbläschen, auch Alveolen genannt, betroffen. Besonders schwerwiegend ist die Form der idiopathischen Lungenfibrose (idiopathische pulmonale Fibrose, IPF). Bei allen Formen der pulmonalen Fibrose ist das Lungengewebe irreversibel geschädigt: Lungenfibrose ist nicht heilbar. Mithilfe entsprechender Therapie- und Pflegemaßnahmen kann der Krankheitsfortschritt jedoch verlangsamt und die Lebensqualität der Patienten möglichst lange aufrecht erhalten werden.
Lungenfibrose: Symptome und Verlauf
Krankheitsverläufe sind prinzipiell variabel. Doch jede Form der pulmonalen Fibrose verläuft zu Beginn unbemerkt. Es können Monate bis Jahre vergehen, bis sich spürbar erste Symptome zeigen. Meist handelt es sich dabei um einen trockenen Reizhusten und Luftnot in Belastungssituationen. Im weiteren Verlauf verlagert sich die Luftnot, in Fachkreisen auch Dyspnoe genannt, in Ruhesituationen. Differentialdiagnostisch zeigt sich die Dyspnoe vor allem in der Einatmung (Inspiration). Im Gegensatz dazu leiden Menschen mit COPD, an Dyspnoe in der Ausatemphase (Exspiration). Der Gasaustausch ist durch die, mit der Vernarbung einhergehende, reduzierte Lungendehnbarkeit und der Veränderung der Membranen der Alveolen, verringert. Sprich, die Aufnahme von Sauerstoff in das Blut und die Abgabe von Kohlendioxid aus dem Blut sind beeinträchtigt. Dies wirkt sich zusätzlich auf die Lungenfunktion aus und bringt weitere Symptome mit sich. Ist die Sauerstoffversorgung im Körper zu gering tritt eine Blaufärbung von Lippen und Fingern auf. Gerade bei einem chronischen Sauerstoffmangel können sich zusätzlich sogenannte Trommelschlegelfinger und Uhrglasnägel ausbilden. Beide treten häufig vergesellschaftet auf. Als Ersteres werden kugelförmig aufgetriebene Fingerendglieder bezeichnet, man nennt Trommelschlegelfinger daher auch als Kolbenfinger.. Die Fingernägel sind hierbei auffällig gewölbt. Durch die Einschränkung der Lunge kommt es im Verlauf oftmals gehäuft zu Infektionen in den Atemwegen. Dies kann als zusätzliches Symptom gedeutet werden. Müdigkeit, Abgeschlagenheit, leichtes Fieber, Muskel- und Gelenkbeschwerden, Appetitlosigkeit und Gewichtsverlust sind, gerade im fortgeschrittenen Stadium, weitere mögliche Symptome. Die Veränderungen in der Lunge bedingen in der Lungenarterie einen vermehrten Rückstau von Blut. Bei dem sich entwickelnden Lungenhochdruck wird vor allem das rechte Herz belastet. Als Reaktion auf diese Überlastung kann sich ein Cor pulmonale (ein Herz, dessen rechte Herzkammer stark erweitert ist – auch Lungenherz genannt) ausbilden. Eine weitere, aber eher seltene Erscheinung, ist das “door-stop”-Phänomen, welches im Allgemeinen auch als Atemstopp bekannt ist. Hierbei kommt es zu einem plötzlichen Stopp des Inspirationsvorgangs, welches nach einigen Inspirationsversuchen wieder verschwindet.
Basis aller Lungenfibrosen ist die Reaktion auf eine sich wiederholende Entzündung im Interstitium und in den Alveolen. Die feinen Wände der Alveolen werden durch die entzündlichen Prozesse in Bindegewebe umgebaut. Dieser Umbau ist die eigentliche Fibrose. Vernarbungen und Verhärtungen der Alveole und der umgebenden Blutgefäße sind die Folge. Die Fläche für den Gasaustausch reduziert sich. Daraus resultiert eine Diffusionsstörung. Das bedeutet, dass Sauerstoff schwieriger vom Körper aufgenommen werden kann. Die Abgabe von Kohlendioxid bleibt aufgrund seiner besseren Diffusionseigenschaft vorerst erhalten. Im weiteren Verlauf ist die Kohlendioxidabgabe ebenso reduziert. Zusätzliche verliert die Lunge an Dehnbarkeit. Der strukturelle Umbau erfolgt auch in den kleinen Bronchien und versteift diese. Nun wird mehr Kraft benötigt, um die Lunge auszudehnen, was einen Anstieg der Atemarbeit zur Folge hat. Die Atmung wird oberflächlich und schneller. Im Verlauf der Erkrankung wird immer mehr Organgewebe in funktionsloses, vernarbtes Gewebe umgewandelt. Diese Veränderung des Lungengewebes ist nicht mehr umkehrbar. Die Lungenfunktion ist negativ beeinträchtigt, was zu der Vielzahl an Symptomen der Lungenfibrose führt. Werden die Ursachen, beziehungsweise die Risikofaktoren, nicht minimiert oder abgestellt, so erfolgt das Fortschreiten der Erkrankung bis zu seinem Endstadium. In der Pneumologie wird die Lunge dann als Wabenlunge (Honey Comb Lung) bezeichnet.
Unsere Stellenangebote für Berlin und Hamburg
Ursachen und Risikofaktoren einer Lungenfibrose
Bei einigen Formen der Lungenfibrose ist die Ursache noch nicht bekannt. Bei vielen anderen Formen sind eindeutige Ursachen und Risikofaktoren identifiziert. So gehört die Inhalation einer Vielzahl von Gefahrstoffen zum klassischen Auslöser eines fibrotischen Umbaus. Gefahrstoffe können als Dämpfe, Aerosole, Gase, Stäube (zum Beispiel Quarzstaub, Asbeststaub, Aluminiumstaub und Berylliumstaub) schädlich wirken. Gerade hohe und langanhaltende Belastung mit diesen anorganischen Stoffen, führen zu Schädigungen in den Zellen des Interstitium. Eine weitere Gefahr kommt aus Richtung der zunehmenden Allergien in unserer Wohlstandsgesellschaft. Die Fibrose gilt als ein mögliches Spätstadium. In Folge von möglichen Bestrahlungstherapien bei Krebserkrankung o. ä. ist ebenso eine fibrosierende Lungenerkrankung (Strahlenfibrose) möglich. Auch Medikamente, wie bestimmte Schmerzmittel, sowie Antibiotika und Medikamente gegen Herzrhythmusstörungen zeigen einen Zusammenhang zur Lungenfibrose. Unabhängig von diesen Risikofaktoren, sind Krankheitsbilder die Narbenbildung der Lunge begünstigen nennenswert. Dazu zählen andere chronisch entzündliche Erkrankungen (Sarkoidose oder, Amyloidose), aber auch rheumatische Prozesse (systemische Sklerose). Wie vorab bereits erwähnt sind Fibrosen in der Lunge ohne erkennbare Ursache als idiopathische Lungenfibrose (IPF) bekannt. Es wird eine Inzidenz von 3-9 (Neuerkrankungen je 100.000 Einwohnern pro Jahr) angenommen. Auf seiner Website beschreibt der Lungeninformationsdienst, dass das Rauchen der einzige zweifelsfrei anerkannte exogene Risikofaktor ist und das Risiko zur Ausbildung einer idiopathische Lungenfibrose etwa verdoppelt.
Diagnosestellung der Lungenfibrose
Bei einem ärztlichen Anamnesegespräch wird das berufliche und private Umfeld nach möglichen Belastungen beleuchtet. Vorhergehende Erkrankungen werden besprochen und aktuelle Beschwerden erfasst. Welche anfänglichen Symptome, wie Reizhusten oder Atemnot, sind wie oft und stark vertreten. Eine körperliche Untersuchung ist obligatorisch und dient unter Anderem der Feststellung eines arteriellen Sauerstoffmangels. Symptome dieses Mangels können vermehrte Inspirationsgeräusche bei der Auskultation, Trommelschlegelfinger und eine bläulich verfärbte Haut (z. b. an den Lippen) sein. Um die Diagnose der Lungenfibrose zu bestätigen und ähnlich oder andere Lungenerkrankungen (z.B. Lungenemphysem) auszuschließen, erfolgen weitere diagnostische Untersuchungen, wie ein Lungenfunktionstest (Spirometrie), eine Untersuchung der Diffusionskapazität und eine Blutgasanalyse. Bei der Spirometrie werden mobilisierbare Luftmengen und Atemflussgeschwindigkeiten gemessen. Das reduzierte Lungenvolumen zeigt sich in der Spirometrie als verminderte Vitalkapazität. Sie ist die Volumendifferenz, welche zwischen maximaler Inspiration und maximaler Exspiration gemessen wird und bildet einen wichtigen Marker zur Diagnostik. Bei der Untersuchung der Diffusionskapazität wird die Fähigkeit zum Gasaustausch bewertet. Sprich, wie gut ist die Sauerstoffaufnahme und wie gut ist die Kohlendioxidabgabe. Die Diffusionskapazität zeigt sich bei der Lungenfibrose erniedrigt. Bei der Blutgasanalyse wird der Sauerstoffgehalt im Blut in Ruhe und auch gegebenenfalls unter Belastung gemessen. Diese Untersuchungen zählen zur Standarddiagnostik. Eine Blutentnahme wird meistens zur Differentialdiagnostik von rheumatischen Erkrankung und Sarkoidose durchgeführt. Ist der erste Teil der Diagnostik abgeschlossen, erfolgen im weiteren Verlauf bildgebende Verfahren der Lunge (Röntgen, Computertomografie oder Magnetresonanztomografie), die ein mögliches Ausmaß der Lungenfibrose darstellen sollen. In diesen häufig bei Lungenerkrankungen eingesetzten Untersuchungen findet bereits eine abgrenzende Diagnostik statt. Eine Lungenspiegelung (Bronchoskopie), mit Entnahme von Gewebeproben, kann weiteren Aufschluss zur Ursache der Beschwerden geben.
Behandlung, Therapie und Pflege bei Lungenfibrose
Nach der Diagnosestellung erfolgt die Empfehlung einer geeigneten Therapie durch das behandelnden ärztliche Fachpersonal. In erster Linie hat die Therapie das Ziel, den Umbau der Lunge zu stoppen oder zumindest den Prozess der Fibrosierung zu verlangsamen. Symptome sollen gelindert und Folgeerkrankungen verhindert werden. Sofern die Ursache bekannt ist, sollte ihr Einfluss sofort abgestellt oder vermieden werden. Zusätzliche Wirkung von weiteren Risikofaktoren sind ebenfalls zu vermeiden. Weitere Maßnahmen, die zur Behandlung von Lungenfibrose eingesetzt werden, sind:
Medikamente bei Lungenfibrose
Grundsätzlich wird mit einer medikamentösen Therapie gestartet. Hierbei werden vorrangig Steroide verordnet, welche die Entzündungen hemmen sollen. Diese Stoffe sind ähnlich dem körpereigenen Hormon Cortisol und wirken antiallergisch und antientzündlich. Die Applikation kann als Inhalation, oral mit Tabletten, als Injektion oder als Infusion erfolgen. Unter Anderem können zudem, gerade bei rheumatischen Beschwerden, Immunsuppressiva zum Einsatz kommen.
Antibiotika bei IPF
Bei bakteriellen Entzündungen hilft eine Antibiotikatherapie. Laut Lungeninformationsdienst sind in den letzten Jahren zwei spezielle Medikamente für die idiopathische Lungenfibrose zugelassen worden. Eine Heilung sei durch diese Medikamente aber nicht möglich.
Sauerstofftherapie für Lungenfibrose-Patienten
Eine weitere zusätzliche Therapieoption ist die Sauerstofflangzeittherapie (LTOT/LOT = Long Term Oxygen Therapy). Hierbei steht vor allem die Behandlung der Hypoxämie, der Sauerstoffarmut im Blut im Vordergrund. Durch die strukturellen Veränderungen der Lunge ist die Sauerstoffaufnahme herabgesetzt. Wird dabei ein bestimmter Grenzwert im Blut unterschritten, so besteht eine Indikation einer Sauerstofflangzeittherapie. Ziel ist die Förderung der Sauerstoffaufnahme im verbleibendem Gasaustauschgebiet

Die Gabe von Sauerstoff kann Lebensqualität bei pulmonaler Fibrose verbessern | © ZBI Gruppe
Weitere Therapien bei Lungenfibrose
Im weitesten Sinne ist die pneumologische Rehabilitation als Therapieform zu benennen. Die Verbesserung der Lebensqualität wird mit einem multimodalen Ansatz verfolgt. Lungensport führt gezielt zu einem Ausbau der Muskulatur und Ausdauer. Auch Atemgymnastik und Atemtherapie können zu einem positiven Effekt in der Lunge führen. Als Ultima Ratio kommt auch eine Lungentransplantation in Betracht. Werden alle Kriterien einer Lungentransplantation erfüllt, so kann dies eine erfolgsbringende Maßnahme sein. Eine Beatmungstherapie ist hinsichtlich der sich stetig reduzierenden Lungendehnbarkeit in Grenzen gesetzt. Beatmung hat primär die Aufgabe als eine Art Zusatzmuskel Luft in die Lunge zu befördern (Ventilation). Der Einfluss von Beatmung auf die Gasaustauscheigenschaften der erkrankten Lunge ist demnach limitiert.

Der Beatmung als Therapieform einer Lungenfibrose sind Grenzen gesetzt | © ZBI Gruppe
So begegnen wir als Pflegende der Lungenfibrose im Endstadium in einem palliativen Setting. Das heißt, die Zielsetzung aller Pflegemaßnahmen dient der Vorbeugung und Linderung von Leid (angelehnt an die WHO Definition).
Lungenfibrose und COVID-19
Bei der Untersuchungen von COVID-19-Patienten an der Charité Berlin wurden Veränderungen gefunden, die der idiopathischen Lungenfibrose ähneln. Dies könnte erklären, “warum die Lungen bei COVID-19-Patienten mit ARDS (acute respiratory distress syndrome) dauerhaft geschädigt werden und eine maschinelle Beatmung oder sogar eine ECMO-Therapie erfolglos bleiben.” (https://www.aerzteblatt.de/nachrichten/129571/COVID-19-Virus-induzierte-Lungenfibrose-erklaert-lange-Beatmungszeiten; abgerufen am 21.04.2022)
Fazit zur Lungenfibrose: nicht heilbar, aber linderbar
Die Lungenfibrose zählt zu den schwerwiegenden und nicht heilbaren Lungenkrankheiten. Die narbigen Veränderungen des Lungengewebes können sich nicht mehr zurückbilden - es ist also nicht möglich die Lungenfibrose zu stoppen. Allerdings kann das Fortschreiten der Krankheit durch konsequente Therapie verzögert werden. Es sollten die bekannten Ursachen und Faktoren in allen Bereichen gemieden werden. Frühzeitige Symptome sollten als diese gedeutet und eine fachärztliche Betreuung aufgesucht werden. Durch die moderne Diagnostik können geeignete Behandlungen besser identifiziert werden. Die Umsetzung und Einhaltung der Therapie ist wichtig für die weitere Lebensqualität und Gesundheit. Eine genaue Prognose der Lungenfibrose ist nicht möglich und von Fall zu Fall unterschiedlich.
FAQ
Was ist der Unterschied zwischen einer Lungenfibrose und COPD?
Während sowohl Lungenfibrose als auch COPD die Atmung beeinträchtigen, liegt der Unterschied in der Art der Lungenschädigung. Bei Lungenfibrose vernarbt und verhärtet das Lungengewebe, wodurch die Dehnbarkeit der Lunge eingeschränkt wird. COPD hingegen verursacht eine Verengung der Atemwege und häufig eine Überblähung der Lungenbläschen. Bei Lungenfibrose ist vor allem die Einatmung erschwert, während COPD die Ausatmung beeinträchtigt.
Welche Symptome deuten auf eine Lungenfibrose hin?
Erste Anzeichen sind meist trockener Reizhusten und Atemnot bei körperlicher Belastung. Später tritt Atemnot auch in Ruhe auf. Weitere mögliche Symptome sind Müdigkeit, Gewichtsverlust, häufige Infektionen der Atemwege, sowie äußerliche Anzeichen wie Trommelschlegelfinger und Uhrglasnägel.
Kann eine Lungenfibrose geheilt werden?
Nein, eine Lungenfibrose ist nicht heilbar. Die Vernarbungen im Lungengewebe sind irreversibel. Allerdings kann der Fortschritt der Erkrankung durch eine frühzeitige und konsequente Therapie verlangsamt und die Lebensqualität der Betroffenen verbessert werden.
Welche Rolle spielt die Sauerstofftherapie bei Lungenfibrose?
Bei fortgeschrittener Lungenfibrose wird die Sauerstoffaufnahme zunehmend beeinträchtigt, was zu Sauerstoffmangel im Blut führt. Eine Sauerstofflangzeittherapie kann helfen, die Sauerstoffversorgung zu verbessern, die Belastbarkeit zu steigern und die Lebensqualität der Betroffenen zu erhöhen.
Was ist eine Wabenlunge und wie entsteht sie?
Eine Wabenlunge (Honeycomb Lung) ist ein fortgeschrittenes Stadium der Lungenfibrose, bei dem das Lungengewebe durch ausgedehnte Vernarbungen so stark verändert ist, dass die Lungenbläschen ihre Funktion verlieren und wie kleine ""Waben"" aussehen. Dieser Zustand ist irreversibel und führt zu einer weiteren Verschlechterung der Lungenfunktion.
Lars Dufeldt ist ausgebildeter Gesundheits- und Krankenpfleger sowie Atmungstherapeut (DGP). Seine Weiterbildung bei der DGP schloss er mit der besten Facharbeit des Jahrganges ab und ist seitdem als Fachbereichsleiter für pneumologische Langzeitrehabilitation im Zentrum für Beatmung und Intensivpflege tätig. Über diese Tätigkeit hinaus besitzt Lars auch eine Weiterbildung zur Pflegefachperson für neurologische Langzeitrehabilitation und verknüpft sein Wissen aus beiden Fachbereichen zum Wohl unserer Klienten und Klientinnen mit außerklinischen Beatmungs- und Intensivpflegebedarf an unseren Standorten Berlin und Hamburg.
Weitere interessante Artikel:
Lungenemphysem » Krankheitsbild und Therapie
COPD » Krankheitsbild, Diagnose & Versorgung
Blutgasanalyse » Grundlagen und Durchführung einer BGA